こんにちは!
それでは今回も化学のお話やっていきます。
今回のテーマはこちら!
動画はこちら↓
動画で使ったシートはこちら(polymerization characteristics 1、polymerization characteristics 2)
では参ります!
低分子合成反応との違い
まずは、低分子と高分子でその合成にはどのような違いがあるのかをお話していきます。
とは言っても、さまざまな合成法があるので、すべてを細かく議論することはしません。
ここでは、決定的に異なるある1点について考えます。
それは、許容できる反応率です。
低分子の合成反応の場合、材料の量から想定される最大の量に対して、その\(\displaystyle 80\sim 90\%\)の量が得られたら、十分優れた反応であると言えます。
しかし、高分子の場合は、ほぼ\(100\%\)の反応率でないといけません。
つまり、副反応が起こってはいけないという条件下でないと作ることができません。
例えば、ビニル化合物の多量体について、その理由を考えてみましょう。
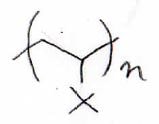
二量体ができる確率を\(\displaystyle 90\%\)だとします。
このとき、三量体を作るためには二量体を作る反応が2回起こればいいので、その反応率は\(\displaystyle 81\%\)になります。
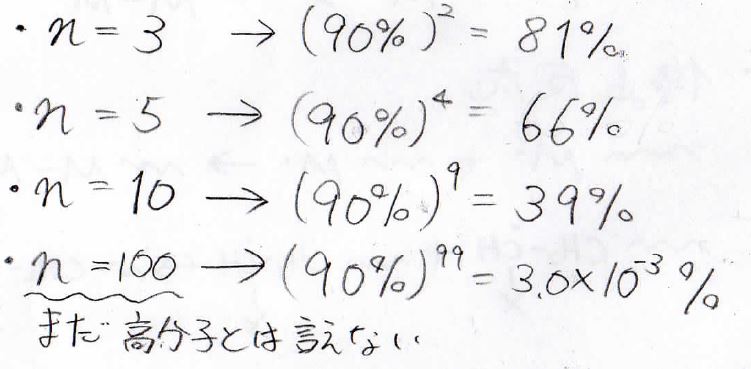
もっと大きな\(\displaystyle n\)量体を作るためには、反応率\(90\%\)の反応を\(\displaystyle n-1\)回繰り返さなければならないので、例えば、\(\displaystyle 100\)量体ができる確率は\(0.003\%\)になります。
ちなみに高分子と呼ぶには、\(\displaystyle 10000\)を超える分子量が必要なので、\(\displaystyle 100\)量体ではまったく高分子とは言えません。
仮に、2量体ができる反応の反応率を\(p\)として\(\displaystyle 1000\)量体ができる確率を計算してみると、このように\(99\%\)と\(99.9\%\)という違いでも、収率におよそ10000倍の差が生じることになり、本当に\(100\%\)に近い反応率でない限り大きな分子を得ることはできないことがわかります。
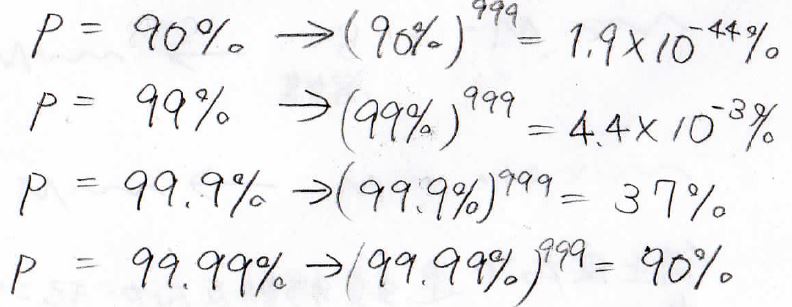
そして、低い反応率は生成してできた高分子の構造の乱れ、多くは広い分子量分布による強度の減少などを引き起こします。
ものによりますが、反応率を高くするために\(150^\circ \rm{C}\)とか、それよりさらに高い温度で合成をしようとすると、生成した多量体が熱分解したり異性化したりするので、目的のものではないものが得られることがあります。
そのため、触媒を使って活性化障壁を小さくしつつ、比較的温和な条件、副反応がほとんど起こらない反応で合成をすることが一般的です。
連鎖重合と非連鎖重合
次に、その高分子を作る反応の分類について、説明します。
まず、高分子を作る反応で最も主流なのは重合反応というもので、これは繰り返し単位となるモノマーに類似の反応を何回も繰り返し起こすことで高分子量体を得る反応のことを言います。
そしてこの重合反応は、連鎖重合と非連鎖重合に分類することができます。
非連鎖重合は、段階重合とも言います。
この2つで何が違うのかを模式的に説明したのが、下の図です。
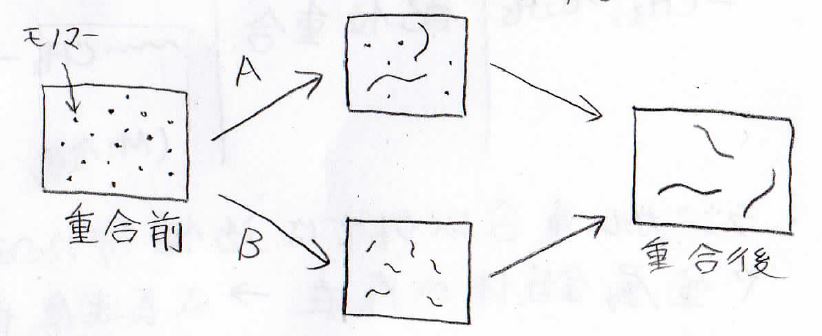
両者の違いは、モノマーがポリマーになる過程にあります。

まず、連鎖重合では活性種とモノマーの間でのみ反応が進行して、モノマーどうしで勝手に反応が起こることはありません。
モノマー濃度は徐々に減少していきます。
活性種ができると、そこを起点に重合が急速に進行していき、あるところで勝手に重合が止まるため、反応にかける時間と分子量にはほとんど関係がありません。
一方の非連鎖重合では、重合が完了する前の時点で短い鎖がたくさんできています。
モノマー同士で重合が起こるため、反応初期では\(\displaystyle 2\)量体や\(\displaystyle 3\)量体がたくさんある状態となりますが、多量体はほとんどできません。
オリゴマーどうしでも重合が起こるため、時間をじっくりかけることで徐々に鎖の本数が減っていき、分子量が大きくなっていきます。
反応を始めた初期段階にほとんどのモノマーが\(\displaystyle 2\)量体になってしまうため、この反応途中のモノマー濃度は、ほぼ\(0\)になります。
この違いは合成にかかる時間やできるポリマーの分子量分布に大きな差を生じさせることになります。
ビニル化合物連鎖重合の分類方法
さらに、ビニル化合物の連鎖重合は、活性種の種類によって、ラジカル重合、カチオン重合、アニオン重合、配位重合に分類できます。
下記のビニル化合物重合反応の一般式において、官能基\(\displaystyle \rm{X}\)によってどの重合方法が適しているのかが変わります。

その対応表は、下のようになります。
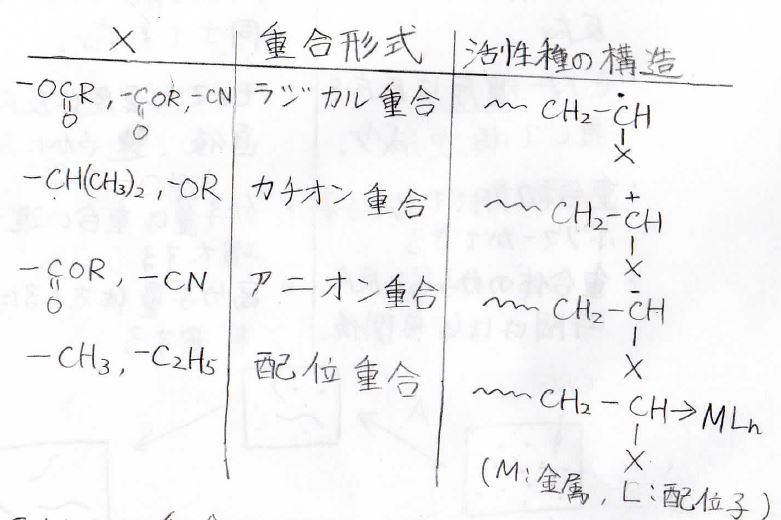
\(\displaystyle \rm{X}\)がその重合方法に適した官能基で、一番右には活性種の構造を書いています。
いずれも成長鎖の末端炭素がラジカルやイオンなど反応性に富む部分になっています。
これがまたほかのビニル化合物のモノマーに付加することで鎖が長くなっていきます。
そして、詳しくはまた別の記事でやっていきますが、ラジカル重合以外では活性な末端付近に対イオンや金属錯体が存在しているため、これが反応速度や立体構造に大きな影響を与えます。
配位重合に使われる錯体はいくつもあり、最も有名なのが左側のZiegler-Natta触媒と呼ばれるものです。
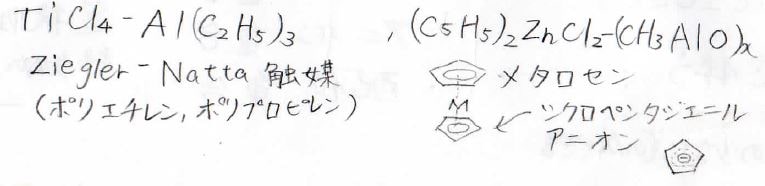
これは、高密度のポリエチレンやポリプロピレンを作るための触媒として知られています。
また、別パターンとしてメタロセンを使うこともあります。
メタロセンというのは右側のように金属イオンが2つのシクロペンタジエニルアニオンに挟まれた構造をもっている錯体の総称になります。
また、この分類とは別にリビング重合というものがあります。
これは、活性種の反応性に著しい選択性があることでモノマーを完全に消費しきった後でも活性種が消失しない、そんな連鎖重合のことを指します。
そして、ラジカル重合でかつリビング重合であればリビングラジカル重合などと呼びます。
リビング重合では、非常に分子量分布の狭いきれいな高分子が得られるので、研究対象として扱いやすく、高分子特有の物性の解明や繊細な材料設計には非常に有用な技術になります。
詳しくはまた別の記事でやりますので、言葉だけでもぜひ知っておいてください。
ラジカル重合の素反応
続いて、これら連鎖重合がどのような素反応によって進行していくのかをお話ししていきます。
この内容は、高分子科学の基本中の基本なので、今後何回も出てくることになると思います。
連鎖重合の素反応は、大きく分けて4つあります。
順番に見ていきましょう。
開始反応
まず、活性種ができる反応を開始反応と言います。
連鎖重合では、活性種とモノマーの間で重合が進行するので、活性種ができることが重合開始のトリガーになります。
ここではラジカル重合を例にお話ししていきますが、ラジカルを発生させて、ラジカル重合のトリガーとなる試薬をラジカル開始剤といいます。

ここで、\(\displaystyle \rm{I}\)はヨウ素ではなくて、英語で開始剤を指すinitiatorからとっています。
ラジカル重合についてはまた別の記事で詳しくやりますが、ラジカル開始剤を1つ紹介しておくと、こちらのAIBNが有名です。
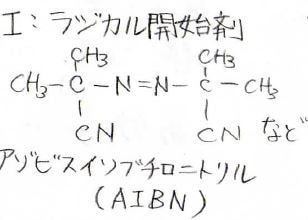
正式名称はアゾビスイソブチロ二トリルという\(\displaystyle \rm{N=N}\)結合をもつアゾ化合物です。
この結合は不安定であり、熱や光によってホモリシス開裂しやすいので、これを利用してラジカルを作ります。
発生したラジカルは、近くのビニルモノマーに付加して、末端の炭素原子が活性となります。
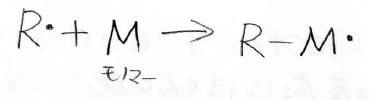
成長反応(生長反応)
開始反応に続いて起こるのが成長反応です。
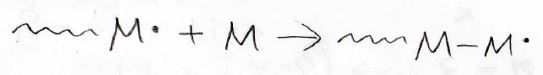
成長鎖がモノマーに付加して、成長鎖が長くなっていきます。
停止反応
次に紹介する停止反応は、開始反応とは反対に活性種が消滅する反応です。
ラジカル重合では再結合と不均化という2つの機構があります。
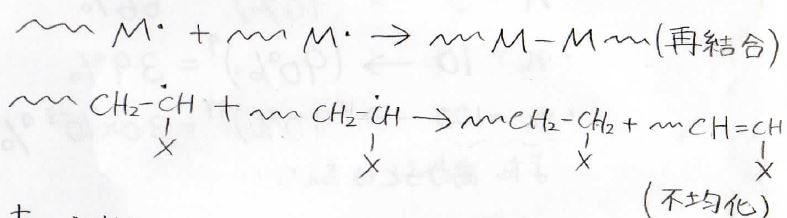
再結合では、2つのラジカルが電子を1つずつ出し合って新たな共有結合を作り、1つの分子になります。
対して不均化では、2つのラジカル間で水素原子を1つ受け渡すことで、異なる2分子ができます。
これらの反応が優勢の場合、すぐに重合が止まってしまうので、高分子量体は得にくいことになります。
連鎖移動反応
そして、最後の素反応が連鎖移動反応です。
この反応では、ラジカルが消滅するのではなく、ほかの分子に活性が移動します。
これは成長鎖とモノマー、そして溶媒分子との間でも起こります。
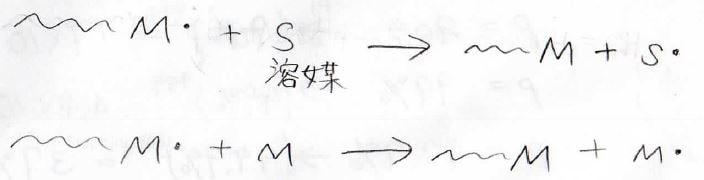
ここで\(\displaystyle \rm{S}\)は硫黄ではなく、溶媒を指すsolventの略です。
この反応では、ラジカルが消滅しないまま、成長鎖の活性だけが失われます。
この反応が多く起こった場合にも高分子量体が得られにくいということになります。
以上はラジカル重合の場合でしたが、イオン重合や配位重合でも似たような機構となります。
ただし、対イオンや錯体の存在によって少し複雑になりますので、ぜひ知っておいてください。
ヘテロ原子を主鎖に含む高分子の重合
続いて、ビニル化合物以外の重合も見ていきます。
ここで考えるのは、主鎖にヘテロ原子を含む高分子の重合です。
ヘテロ原子というのは炭素、水素原子以外の原子のことです。
連鎖的な重合法
これを連鎖重合で作ろうとした場合は、開環重合という反応が有用です。
環状のモノマーが開環を繰り返しながら重合が進行していきます。

なぜこのような反応が進行するのかということを、反応ギブズエネルギーで説明すると、次のようになります。

環状化合物は、その環員数によっては安定な結合角をとれず、結合角に大きくひずみがかかっています。
環がなくなることでその結合角ひずみが解消するため、発熱反応であり、反応エンタルピーは負の値になります。
その安定化がエントロピーの減少分を上回り、反応ギブズエネルギーが負となった場合に反応は進行します。
非連鎖的な重合法
では今度、ヘテロ原子を主鎖に含むポリマーを非連鎖重合で作る方法を紹介します。
重縮合
高校でも習うので、こっちの方が開環重合より有名だと思いますが、まずは重縮合があります。
例えば、アミノ酸であるグリシンのアミノ基とカルボキシ基が繰り返し反応することで、ポリグリシンが生成します。

このとき、水という低分子の脱離が伴います。
水に限らず、このように重合とともに低分子が脱離していく反応のことを重縮合と言います。
重縮合は別名、縮合重合、縮重合ともいいます。
ちなみに、ポリグリシンは2個の炭素を繰り返し単位にもつポリアミドなので、ナイロン2と呼ぶこともできます。
重付加
非連鎖重合のもう1つ代表的なものが重付加です。
こちらの反応では、低分子の脱離を伴わずに重合が進行していきます。
代表的なのはジイソシアナートとジオールをつかったポリウレタンの合成です。
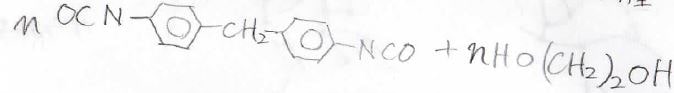
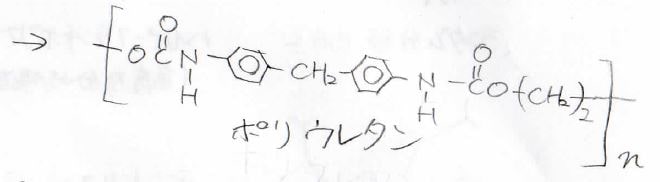
重付加は付加重合とも言います。
縮合的連鎖重合
少し変わったパターンも紹介しておきます。
開環反応と重縮合が組み合わさった縮合的連鎖重合というものもあります。
\(\displaystyle \alpha\)-アミノ酸のアミノ基の一方の水素原子がカルボキシ基になって、そこから水が脱離したNCAという化合物を重合することでポリペプチドが得られます。
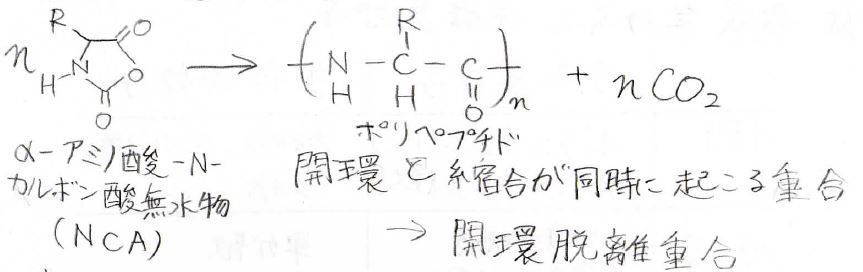
そのとき、二酸化炭素が脱離します。
このように、重縮合でも開環を伴う場合には、連鎖重合となる場合があります。
この反応は開環脱離重合とも言います。
カルボニル、イミンの連鎖重合
アルデヒドやケトンといったカルボニルおよびイミンでも連鎖重合を考えることができます。
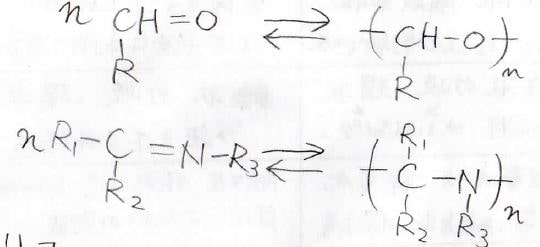
しかし実際は、多量体とモノマーおよびオリゴマーが化学平衡となり、解重合が起こってしまうため、高分子を得るのは難しいです。
シリコン(ポリシロキサン)の重合
最後に、シリコン(ポリシロキサン)の合成について、お話しします。
シリコンはその分子量によって液状、ゴム状、樹脂と形を変え、さらに成形加工の容易さや耐薬品性などの優れた性質により、様々な用途に使われている材料です。
これを作るためには、下のような反応を起こします。
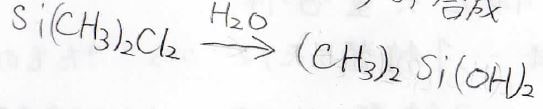
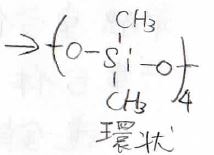
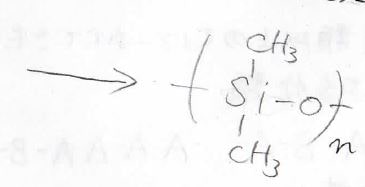
3段階目でいったん環を形成してから重合するというのが特徴的な反応です。
まとめ
今回の内容は以上です。
間違いの指摘、リクエスト、質問等あれば、Twitter(https://twitter.com/bakeneko_chem)かお問い合わせフォームよりコメントしてくださると、助かります。
それではどうもありがとうございました!