こんにちは!
今回のテーマはこちらです!
動画はこちら↓
動画で使ったシートはこちら(alcohol 5)
では早速行きましょう!
アルコール+強塩基
まず、アルコールに強塩基を加えた場合から考えていきます。
この場合は、アルコールが酸としてはたらくので、塩基によってプロトンが引き抜かれてアルコキシドが生成します。
そのため、求核置換も脱離も起こりません。
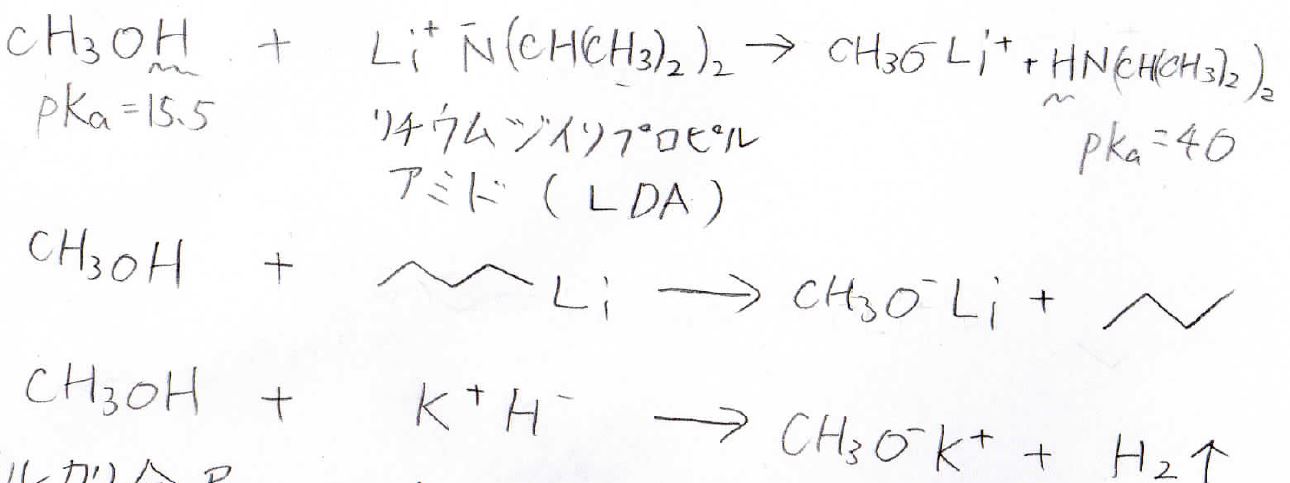
ここで1つ、有名な試薬を紹介しておくと、リチウムジイソプロピルアミド、通称LDAというものがあります。
これは嵩高い強塩基の代表例で、求核置換反応させたくないときに使えます。
アルコール+アルカリ金属
少し変わったパターンとして、アルコールとアルカリ金属を反応させた場合も、アルコキシドができます。

この場合は還元を伴っており、水素ガスが発生します。
水とアルカリ金属の反応はとても激しくて危険なのですが、アルコールとの反応はそこまで激しくなくて、第三級アルコールとの反応が最も穏やかになります。
実際に、未反応の金属カリウムがまだ残っているときには、上記の2-メチル-1-プロパノールと穏やかに反応させて、安全に処理するという方法があります。
アルコール+ハロゲン化水素
続いて、アルコールとハロゲン化水素の反応を見ていきましょう。
直鎖状第一級アルコール+ハロゲン化水素
まず第一級アルコールとの反応では\(\displaystyle \rm{S_N2}\)反応が起こります。
とは言っても、水酸化物イオンの脱離能はとても小さいので、違うものが脱離することになります。
こちらが反応機構です。

まず、アルコールの酸素原子上にある孤立電子対がハロゲン化水素からプロトンを引き抜いて、カチオン種になります。
その後、ハロゲン化物イオンが背面から求核攻撃すると、電子がこのように移動して、水が脱離します。
水酸化物イオンとしての脱離能はとても小さいですが、水としては、優れた脱離基になります。
この反応は、高濃度のヨウ化水素と臭化水素でうまく進行しますが、塩化水素での反応はあまり有利ではありません。
フッ化水素は弱酸なので、ほとんど反応しません。
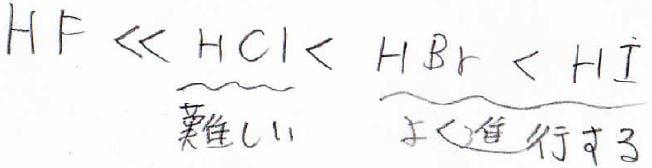
第二級、第三級アルコール+ハロゲン化水素
では続いて第二級、第三級アルコールとハロゲン化水素の反応を考えます。
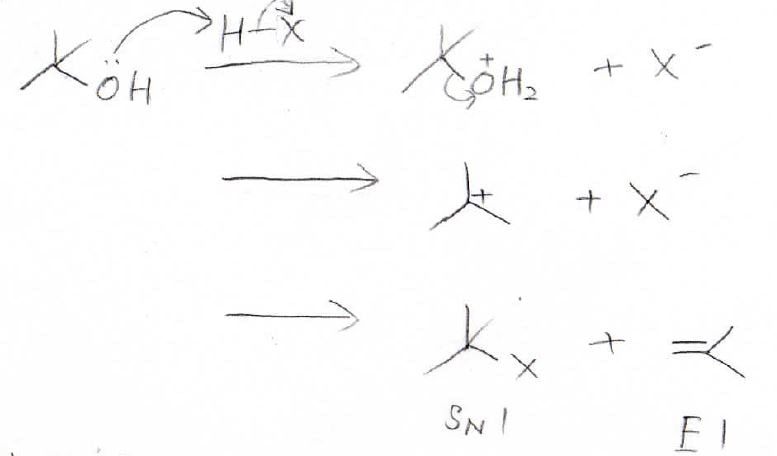
この組み合わせでは、\(\displaystyle \rm{S_N1}\)と\(\displaystyle \rm{E1}\)が進行します。
すなわち水の脱離が起こって中間体としてカルボカチオンを経る反応となります。
ハロゲン化水素ではなく、もっと高温条件で非求核性の酸を使った場合には、\(\displaystyle \rm{S_N1}\)が抑制されるので、\(\displaystyle \rm{E1}\)が有利に進行し、このようにアルコールを脱水することができます。
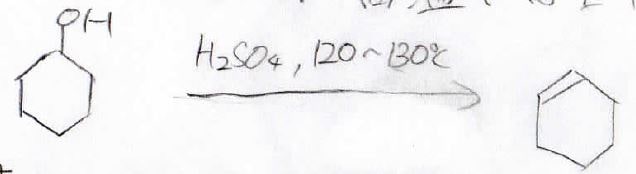
カルボカチオンでは、より安定な第三級アルコールになるために、\(\displaystyle \rm{H}\)や\(\displaystyle \rm{CH_3}\)の転位が起こる可能性があります。

分枝のある第一級アルコール+ハロゲン化水素
また、これはかなりの例外なのですが、分岐のある第一級アルコールでも、アルキル移動が起こることがあります。
反応機構は以下のとおりで、第一級カルボカチオンを経由することなく、水の脱離とアルキル移動が協奏的に起こります。

本来、第一級カルボカチオンはきわめて不安定ですが、見かけ上転位が起こっているような反応が起こることがあります。
練習問題
最後、練習問題をやってみましょう。
以下の2つの反応で、主生成物はどのような構造になるでしょうか?
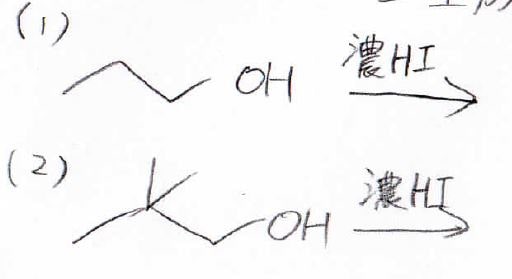

(1)は直鎖上の第一級アルコールとハロゲン化水素の反応です。
まず初めにアルコールがプロトンを引き抜いた後、ヨウ化物イオンの求核攻撃が\(\displaystyle \rm{S_N2}\)機構で進行するので、結果としてヒドロキシ基がヨウ素に置換されたヨードアルカンとなります。
(2)は先ほどと同じ第一級アルコールとハロアルカンの反応ですが、分枝があります。
この場合は、アルキル移動と水の脱離が協奏的に進行して、第三級カルボカチオンが中間体として生成します。
ここにヨウ化物イオンが\(\displaystyle \rm{S_N1}\)機構で求核攻撃するので、第三級ヨードアルカンとなります。
まとめ
はい、今回の内容は以上です。
間違いの指摘、リクエスト、質問等あれば、Twitter(https://twitter.com/bakeneko_chem)かお問い合わせフォームよりコメントしてくださると、助かります。
それではどうもありがとうございました!




