こんにちは!
今回のテーマはこちら!
動画はこちら↓
動画で使ったシートはこちら(fundamentals)
有機化学とは
有機化学とは、炭素原子を含む化合物を扱う化学の分野です。
最大で4本の共有結合が作れる炭素原子をもつ化合物は、枝分かれや二重、三重結合によって、さまざまな構造をもちます。
それによって発現する物理的な性質の身の回りの生活に役立つだけでなく、生物学や医学の発展にも寄与するため、化学を専攻する人は避けては通れないほど重要な分野だと言えます。
実は、ある有機化学の反応が起こったとして、その反応性を説明する要因は、それほど多くありません。
ここでは、重要な因子をいくつか挙げます。
反応性を変化させる主な要因
共鳴安定化
まず、その化学種が有利な共鳴構造をもつとき、共鳴構造がない場合に比べて、熱力学的に安定となります。
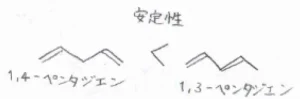
これは、電子が広く分布したことで、クーロン斥力が減少することと、量子力学的な効果によって説明されます。
共鳴については、こちらの記事を参照してください。
電気陰性度
次に、有機化学では電気陰性度の話もよく出てきます。
すべての元素の中で最も電気陰性度の高いフッ素の原子核は、電子を強く引き寄せます。
その結果、例えば、トルエンとトリフルオロメチルベンゼンでは、ベンゼン環内の電子密度に大きな差が生じることになります。
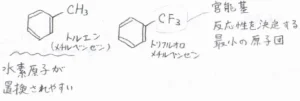
これにより、トリフルオロメチルベンゼンに対する求電子的な反応の速度は、トルエンに比べてとても遅くなります。
この反応については、また別の記事で詳しくやることになります。
トリフルオロメチル基のように反応性を決定する最小の原子団のことは、官能基と呼びます。
立体反発
次に挙げる重要な要素は、立体反発です。
例えば、ヨードメタンと2-ヨード-2-メチルプロパンでは、後者のほうがメチル基3つ分大きな分子です。
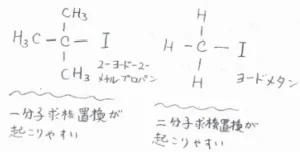
これらに、求核剤と呼ばれる試薬を加えたとき、前者では二分子求核置換(\(\displaystyle \rm{S_N}\)\(2\))、後者では一分子求核置換(\(\displaystyle \rm{S_N}\)\(1\))と言われる異なる機構の反応が起こります。
機構が異なると、反応速度の濃度依存性や立体が保持されるかどうかなどにも違いが生じます。
機構が異なる理由の1つは、立体的に混みあった炭素中心まで反応剤の分子が近づきにくいことによるものです。
このように、反応物の嵩高さが反応性に影響を及ぼすことが多々あります。
安定な立体構造とひずみ
最後に紹介するのは、分子の立体構造です。
量子力学によって導かれる結論として、主量子数が2以上のとき、電子の波動関数として、等方的な\(\displaystyle \rm{s}\)\(\)軌道と異方的な3つの\(\displaystyle \rm{p}\)\(\)軌道が考えられます。
化合物の立体構造を理解するためには、これら4つの軌道を組み合わせた混成軌道の考え方がよく出てきます。

中心の炭素原子から見て、\(\displaystyle \sigma\)結合の本数と孤立電子対数の和が2になるときには、\(\displaystyle \rm{s}\)\(\)軌道と1つの\(\displaystyle \rm{p}\)\(\)軌道が組み合わさった\(\displaystyle \rm{sp}\)\(\)混成軌道を考えます。
\(\displaystyle \sigma\)結合の本数と孤立電子対の和が3のときには、\(\displaystyle \rm{s}\)\(\)軌道と2つの\(\displaystyle \rm{p}\)\(\)軌道から\(\displaystyle \rm{sp}\)\(^2\)混成軌道を作り、\(\displaystyle \sigma\)結合の本数と孤立電子対の和が4のときには、\(\displaystyle \rm{s}\)\(\)軌道と3つすべての\(\displaystyle \rm{p}\)\(\)軌道から\(\displaystyle \rm{sp}\)\(^3\)混成軌道を作ります。
これらは、電子対間の静電反発が最小となるように、互いにできるだけ離れた方向に電子の分布をもちます。
その結果、それぞれの立体構造は、直線型、平面構造、四面体型となります。
混成軌道については、こちらの記事も参照してください。

反応物や生成物だけでなく、その途中で経由する中間体や遷移状態の構造を予想することで、実際の反応をより理解しやすくなります。
そして、有機化合物の中には、こちらに示すような環状のものが存在しています。
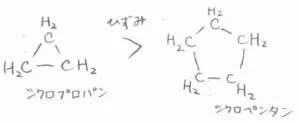
ここに示した化合物の炭素原子はすべて\(\displaystyle \rm{sp}\)\(^3\)混成なので、本来の結合角はおよそ\(\displaystyle 109.5^\circ\)となるはずですが、環を形成するために、そこから大きくひずんだ構造をとっています。
特に、左のシクロプロパンに関しては、正三角形の角の大きさは\(\displaystyle 60^\circ\)であることから、およそ\(\displaystyle 50^\circ\)も結合角にストレスがかかっていることになります。
したがって、シクロプロパンは、右のシクロペンタンよりも熱力学的に不安定であり、より反応性に富む化合物だと言えます。
環を形成しているどこかの共有結合を解離させれば、蓄積されていたエネルギーが放出されるので、それが反応が起こるきっかけになることも多いです。
以上が、有機化学の反応性を左右する主要な要素でしたが、超共役など、まだお話できていないこともあるので、必要なときにお話ししていきます。
有機化学で出てくる基本的な概念
ここからは、有機化学で基本的な概念をいくつかピックアップしていきます。
共有結合の原理
まず、共有結合が形成される原理についてです。
まず古典的には、正の電荷をもつ原子核と負の電荷をもつ電子の間に静電的な引力がはたらくことで、分子は安定化していると考えられます。
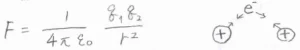
ただし、これだけでは原子が分子を形成することの説明には不十分で、1つの電子が2つの原子核の間で交換されることによる量子力学的な効果が大きな役割を果たしています。
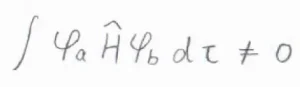
ここについては、こちらの記事を参照してください。
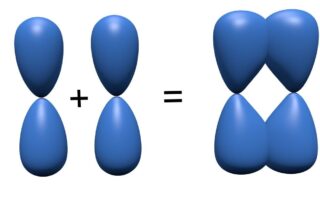
それぞれの原子から軌道を1つずつ出し合って新たな分子軌道を作ったとき、一方はより安定となる結合性軌道、もう一方はより不安定な反結合性軌道となります。
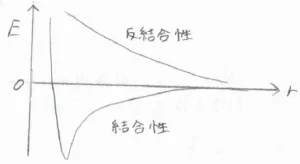
反結合性軌道も、結合が解離するプロセスに関与しており、有機化学においても重要な概念だと言えます。
ある化学結合があったときに、それが共有結合かイオン結合かは完全に分かれているわけではなく、その中間のどこかに位置します。
一般的に、2つの元素の電気陰性度の差が小さいほど共有結合に近く、電気陰性度の差が大きいほどイオン結合に近くなります。
構造式
続いて、化合物の構造の表し方の話をします。
同じ化学式や同じ組成式だったとしても、その構造が全然違うということがよくあります。
そこで、原子がどのように結合していて、空間的にどのように配置されているかを表した構造式で化合物を表すことが多いです。
主要な構造式の書き方として、ここでは2つ紹介します。
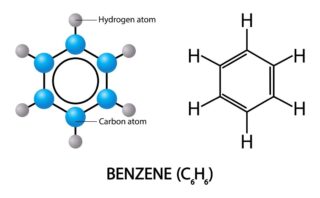
ルイス(Lewis)構造式は、高校化学では電子式と呼ばれているものです。
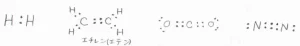
価電子を点で表します。
そして、ケクレ(kekulé)構造式では、共有結合を線で表します。
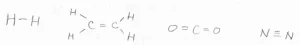
有機化学では、ケクレ構造式を使うのが主流ですが、孤立電子対が関与する反応も多いので、共有結合を線で書きつつ、ルイス構造式のように孤立電子対を点で表して書くことがよくあります。
8電子則(オクテット則)とその例外
ルイス構造式を考えるときには、8電子則(オクテット則)という経験則が役に立ちます。
これは、原子どうしが共有結合を形成するときには、分子中にある原子の最外殻電子数が8個のとき、安定した分子として存在するという法則です。
リチウムとベリリウムを除く第2周期の元素について、特によく当てはまるものです。
ただし、以下のような例外があります。
超原子価化合物
まず、周期表の下にある元素ほどオクテット則は成り立ちにくいです。
形式的に原子価殻に9つ以上の電子をもつ典型元素を含む化合物のことは、超原子価化合物と言います。
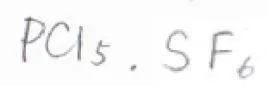
ここに示した五塩化リンや六フッ化硫黄のほか、硫酸分子も超原子価化合物に含まれます。
詳しくは、こちらを参照してください。

水素、リチウム
そして、水素とリチウムについては、最外殻電子数が2個の状態で、安定な分子を形成します。
これを2電子則と言います。
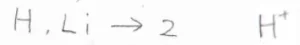
2電子則と8電子則で共通していることは、希ガス(貴ガス)と同じ電子配置になるということです。
希ガスは、電子の分布が対称的であることにより電子間反発が最小化されるため安定となりますが、それと同様の効果が分子内の原子にもあるというイメージです。
また、特殊な例として、最外殻電子が0個の水素イオンもあります。
重水素や三重水素でない水素の原子核は、中性子をもたず、陽子とまったく同じものなので、水素イオンというよりもプロトンという呼び方をするほうが多いです。
ベリリウム、ホウ素
オクテット則のほかの例外としては、電気陰性度の低いベリリウムやホウ素が4電子や6電子でも、そこまで安定とは言えませんが、分子を形成することが知られています。

ここに示した\(\displaystyle \rm{BH}\)\(_3\)という化合物は、ボランと呼びます。
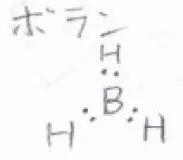
単独だとかなり不安定なので、通常は二量体であるジボランとして存在します。
カルベン
また、周期表の中でホウ素の隣に位置している炭素についても、カルベンと呼ばれる6電子の化学種が存在します。
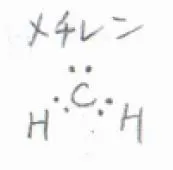
ここには、最も単純なカルベンであるメチレンを書いています。
一般的に、カルベンはとても不安定なので、反応性に富む化学種として知られています。
形式電荷
形式電荷とは、分子中にある原子がもつ見かけ上の電荷のことです。
これはあくまで見かけ上という話で、実際には、電子は雲のように分布しているので、1つの原子上に1個の電子が局在していると考えるのは正しくありません。
それでも、大型計算機を使うことなく、安定な電子の配置を考えたり、電子分布を推定することができるため、今でも重要な概念として残っています。
その一般式は、(遊離した原子の価電子の数)\(\displaystyle -\)(着目している原子上にある孤立電子の個数)\(\displaystyle -\)(結合電子対の数)で与えられます。
例として、ヒドロニウムイオンを考えると、まず水素原子の1つについては、価電子数が\(\displaystyle 1\)、孤立電子数が\(\displaystyle 0\)、結合電子対数が\(\displaystyle 1\)なので、\(\displaystyle 1-0-1=0\)となります。
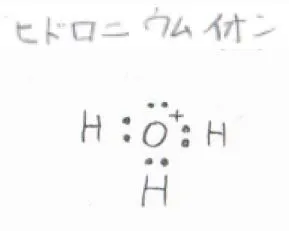
すなわち、形式電荷は\(\displaystyle 0\)で、電気的には中性となります。
同様に、酸素原子について考えると、価電子数が\(\displaystyle 6\)、孤立電子数が\(\displaystyle 2\)、結合電子対数が\(\displaystyle 3\)なので、\(\displaystyle 6-2-3=1\)となります。
形式電荷が正の値をとるとき、その原子は正に帯電していると解釈されます。
このとき、ヒドロニウムイオンの正電荷が酸素原子に局在しているような書き方をします。
以上のようにして、形式電荷から酸素原子中心の電子密度が小さいような電子分布をしていることが予想できます。
電子の移動を表す矢印の書き方
反応機構を表す際、酸化還元反応などの電子の移動は、矢印を使って表します。
分子内の結合ないし原子のうち、電子の移動の始点と終点がどこなのかがわかるように曲がった矢印を使います。
両矢印は電子対の移動、半矢印は1つの電子の移動を表します。

水素分子が2つに分かれる際、結合を形成していた電子が2つとも、一方の水素原子側へ移動すると、水素イオンと水素化物イオンができます。
このような形式の解離は、ヘテロリシス開裂と呼ばれます。
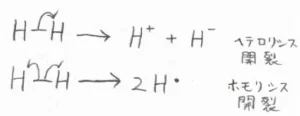
対して、結合を形成していた電子が2つの原子核に1つずつ移動すると、電気的に中性な水素原子が2つできます。
このような形式の解離は、ホモリシス開裂と言います。
また、水素原子のように不対電子をもつ化学種の総称をラジカルと言います。
有機化学の教科書で、結合の強さを議論するときには、結合解離エネルギーという量がよく使われます。
これは、あくまでホモリシス開裂するために必要なエネルギーであり、ヘテロリシス開裂のしやすさまでは測れないので、注意してください。
酸と塩基の定義
続いて、酸と塩基の定義について、お話しします。
ここでは、ブレンステッド-ローリーの定義とルイスの定義の2つを取り上げます。
アレニウスの定義というものもあるのですが、あまり使わないのでここでは取り上げません。
ブレンステッド-ローリーの定義
まず、ブレンステッド-ローリーの定義では、プロトンを与えるものを酸、プロトンを受け取るものを塩基と呼びます。
プロトン性の\(\displaystyle \rm{HA}\)\(\)という仮想の化学種が\(\displaystyle \rm{H}\)\(^+\)と\(\displaystyle \rm{A}\)\(^-\)に解離し、またその逆反応も起こって化学平衡状態となるとき、\(\displaystyle \rm{HA}\)\(\)のことをブレンステッド酸、\(\displaystyle \rm{A}\)\(^-\)のことをブレンステッド塩基と呼びます。

また、\(\displaystyle \rm{HA}\)\(\)は\(\displaystyle \rm{A}\)\(^-\)の共役酸であり、\(\displaystyle \rm{A}\)\(^-\)は\(\displaystyle \rm{HA}\)\(\)の共役塩基であると言います。
活量係数がすべて\(\displaystyle 1\)のとき、平衡定数\(\displaystyle K_\rm{a}\)\(\displaystyle =\frac{[\rm{H}^+][A^-]}{[\rm{HA}]\mathit{c}^\circ}\)となり、\(\displaystyle K_\rm{a}\)\(\)が大きい値であるほど\(\displaystyle \rm{HA}\)\(\)は強い酸であり、\(\displaystyle \rm{A}\)\(^-\)は弱い塩基であることになります。
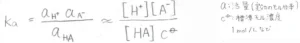
ここで、大かっこはモル濃度を示します。
\(\displaystyle c^\circ\)は標準モル濃度という量で、ここでは\(\displaystyle 1\ \rm{mol\ L}\)\(^{-1}\)だと思ってください。
特に、酸が塩基とプロトンに解離する反応式についての平衡定数のことは、酸解離定数と呼ばれます。
酸解離定数はとりうる値の範囲が広いため、一般的には常用対数にマイナスをかけた\(\displaystyle \rm{p}\)\(K_\rm{a}\)\(\)という指数によって、酸の強さを評価します。
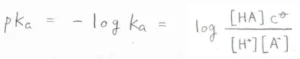
\(\displaystyle \rm{p}\)\(K_\rm{a}\)\(\)が小さいほど強い酸であると言えます。
ルイスの定義
そして、もう一方のルイスの定義によると、電子を受け取るものが酸、電子を与えるものが塩基になります。
例えば、先ほども紹介したボランですが、試薬としてはエーテル溶液の形で売られているのが一般的です。
通常、ボランは二量体であるジボランとして存在しますが、ジボランも反応性が非常に高く、強力な還元作用があるほか、爆発する危険性があるため、試薬として取り扱うことが困難です。
エーテルの一種であるテトラヒドロフラン(THF)溶液であれば、ホウ素原子の最外殻電子数が8個となるように酸素原子から電子が供与されて、安定な錯体を形成します。

そのため、安全な試薬としては、この形が一般的になっています。
この錯形成について、ボランがルイス酸、テトラヒドロフランがルイス塩基にあたります。
分子軌道から考えると、ボランは\(\displaystyle \rm{sp}\)\(^2\)混成で平面構造をしており、その平面に対して垂直な方向に位置している\(\displaystyle \rm{p}\)\(\)軌道には電子がありません。
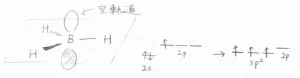
電子が占有していない電子軌道のことは空軌道と呼ばれ、電子の受け渡しはここで行われます。
ルイスの定義を使うと、多くの系について、酸と塩基を決めることができます。
プロトンをルイス酸、水をルイス塩基とみなせば、ブレンステッド-ローリーの定義もルイスの定義に包含されると解釈できます。
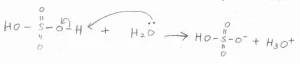
酸性度、塩基性度
最後に、酸の強さが変化する要因についてお話しします。
酸性度が高い(\(\displaystyle \rm{p}\)\(K_\rm{a}\)\(\)が小さい)というのは、共役塩基の塩基性度が低いという意味でもあるので、そのように理解してください。
共役塩基の安定性
まず、共役塩基が熱力学的に安定であるとき、酸性度は高くなります。
例えば、メタノールと酢酸では、プロトンが外れたときにできる陰イオンを考えたときに、酢酸イオンだけ共鳴構造が書けることがわかります。
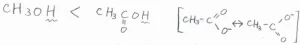
共役塩基が安定であることから、酢酸のほうが強い酸だと推測されます。
もし仮に、共役塩基が熱力学的に不安定であれば、酸性度は低くなります。
電気陰性度
そして、電気陰性度の差からも酸性度に違いが生じます。
ここでは例として、メタンとアンモニアについて考えることにします。

炭素と窒素で、電気陰性度が大きいのは窒素であるため、アンモニアの結合は、メタンの結合よりも分極が大きいです。
窒素原子側に負電荷が集中している分だけ、水素原子の周りの電子密度は小さくなるため、プロトンとしての解離は容易となります。
したがって、アンモニアはメタンよりも酸性度が高いと言えます。
結合距離
一方で、電気陰性度だけでは酸性度の大小関係を見誤ることもあります。
代表的なのがハロゲン化水素の酸性度です。
フッ素が最も電気陰性度が大きい元素なので、フッ化水素の酸性度がいちばん高いと考えられますが、これは誤りです。
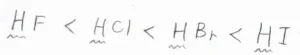
実際には、フッ化水素は弱酸、それ以外のハロゲン化水素は強酸に分類されます。
これには、結合距離が関係しています。
周期表の下にある元素ほど電子の広がりが大きく、分子内の結合距離も長くなる傾向にあります。
結合距離が長いと軌道の重なりが小さいため、結合を形成したことによるエネルギーの安定化が小さくなります。
そのため、ヨウ化水素が最も解離しやすく、最も強い酸であると言えます。
フッ化水素は、結合距離が近いために、そもそも結合としてかなり強く、ホモリシス開裂もヘテロリシス開裂も起こりにくいです。
その結果、フッ化水素だけ弱酸に分類されるほど酸性度は低くなります。
このように、結合距離も酸性度を左右する重要な要素となります。
\(\displaystyle \rm{s}\)\(\)軌道の寄与
\(\displaystyle \rm{sp}\)\(\)混成軌道と\(\displaystyle \rm{sp}\)\(^3\)混成軌道を比べると、\(\displaystyle \rm{sp}\)\(\)混成軌道のほうが\(\displaystyle \rm{s}\)\(\)軌道の寄与が大きいです。
これを\(\displaystyle \rm{s}\)\(\)性が大きいと言います。
\(\displaystyle \rm{s}\)\(\)軌道は、\(\displaystyle \rm{p}\)\(\)軌道に比べて電子の広がりが小さいため、電子が内側に集中した形をとりやすいです。
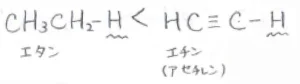
その結果、三重結合をもつ化合物の末端水素の酸性度が高くなります。
まとめ
今回の内容は以上です。
間違いの指摘、リクエスト、質問等あれば、X(https://X.com/bakeneko_chem)かお問い合わせフォームよりコメントしてくださると、助かります。
それではどうもありがとうございました!




