 化学
化学 【大学の物理化学】イオンの活量係数を考えるデバイ-ヒュッケル理論について、わかりやすく解説!
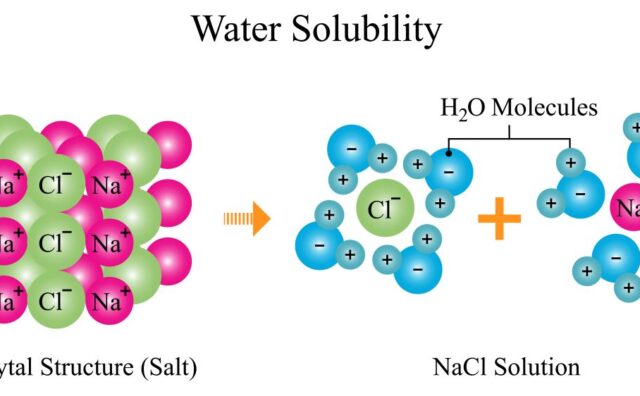
イオンの周りでは、静電相互作用により、反対の電荷をもつ対イオンの濃度が局所的に高くなります。その結果、中心にあるイオンは、遠い位置にあるイオンと相互作用しにくくなります。見かけ上電荷が小さくなるこの現象を静電遮蔽と呼びます。この記事では、電解質溶液中で、静電遮蔽により実効濃度が下がる効果について考えていきます。
 化学
化学  化学
化学  化学
化学  コラム
コラム  化学
化学  化学
化学  化学
化学  化学
化学  化学
化学  化学
化学  化学
化学  化学
化学  化学
化学  化学
化学  化学
化学