こんにちは!
それでは今回も化学のお話やっていきます。
今回のテーマはこちら!
動画はこちら↓
動画で使ったシートはこちら(tacticity)
それでは内容に入っていきます。
高分子に含まれる不斉炭素
まず、下のビニル化合物の重合反応をご覧ください。

このような付加重合では、付加が起こるたびに4つの官能基がすべて異なる不斉炭素ができます(厳密には光学活性にはならないため、擬不斉炭素)。
これらの不斉炭素の並び方が変わると、光学異性体ではない立体異性体、いわゆるジアステレオマーになるため、物性が変わってきます。
そのため、高分子の物性を理解するためには、これら立体化学的な視点が不可欠になるわけです。
それでは、こんなにたくさんある不斉炭素をどのように評価すればよいのでしょうか?
その答えは、隣り合う複数の不斉炭素の立体的関係を見るというものです。
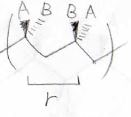
例えば、隣り合う2つの不斉炭素のパターンは次の2パターンがあります。
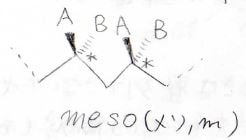
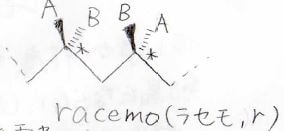
一方は隣り合う不斉炭素の立体が同じ向き、もう一方は異なる向きになっています。
前者のことをmeso(メソ)、後者のことをracemo(ラセモ)と呼び、それぞれmとrで表します。
これらは鏡写しの関係ではないため、物性の違いを生じさせます。
これは単なる言葉の説明ですが、mesoとracemoは連続した2つの不斉炭素の立体的関係を示すものだということで2連子と呼ばれます。
立体規則性
高分子の立体規則性を議論する際には、これら連子の割合を使います。
例えば、下のように不斉炭素が6つ連なった構造であれば、mesoとracemoが2:3となります。
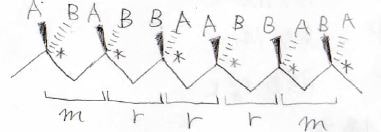
この割合のことは、tacticity(タクティシティ)と言います。
3連子の種類とその呼び方
そして、高分子の立体を議論する際には2連子だけでなく3連子もよく使われます。
つまりは3つ連なった不斉炭素の立体的関係です。
先ほどと同じ配列を例にすると、3連子はこのように2連子を2つ組み合わせることで表せることになります。

それぞれの3連子には名前がついていて、mmはイソタクチック(アイソタクチック)、rrはシンジオタクチック、mrはヘテロタクチックと呼びます。
4連子以上について
2連子、3連子があれば、4連子や5連子もあります。
4連子をmとrで表すと、こちらの6種類を考えることができます。
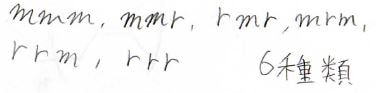
5連子はこの10種類です。
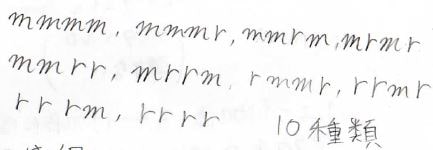
ただし、3連子までとは違って、これらには個々の名前がついていません。
これらを使うことは多くなく、重要度は低いです。
3連子までをしっかり理解しましょう。
立体規則性による分類方法
さあ、ここからは立体規則性による高分子の分類方法についてお話しします。
話は逸れますが、高分子のほかの分類方法もまとめておりますので、ぜひご覧ください。

ここでは、ビニル重合体を例にお話ししていきます。
mmm・・・とmesoがずっと連続する高分子のことは、イソタクチックポリマー(アイソタクチックポリマー)と言います。
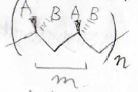
対して、rrr・・・とracemoが連続する高分子は、シンジオタクチックポリマーと呼びます。
そして、mとrが完全にランダムな配列をしている高分子は、アタクチックポリマーと呼びます。
さらに、これがイソプレン重合体になるとより複雑になります。
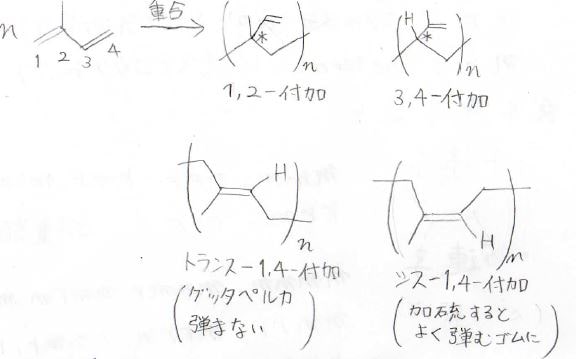
重合形式が1,2-付加、3,4-付加、トランス-1,4-付加、シス-1,4-付加と4つ存在しています。
1,2-付加、3,4-付加については不斉炭素が連なっている構造であるため、ビニル重合体同様にイソタクチック、シンジオタクチック、アタクチックが存在します。
そして、トランス-1,4-付加ポリイソプレンは別名グッタペルカとも呼ばれていて、弾みが少ない材料として主にはゴルフボールのカバーに使われています。
シス-1,4-付加ポリイソプレンは、その立体障害によりよじれた状態で存在しているため、弾性を示します。
加硫することにより優れた弾性をもつ合成ゴムになり、タイヤや生活用品、スポーツ用品として使われています。
ちなみにポリブタジエンの場合は、1,2-付加、トランス-1,4-付加、シス-1,4-付加という3種類の重合形式になります。
立体規則性によって生まれる物性
最後に、立体規則性によってどのような物性の違いが生まれるのかという話をします。
¹H-NMR
まず挙げられるのが¹H-NMRスペクトルにおける違いです。
mesoとracemoの構造をもう一度見てみると、主鎖のメチレン水素2つがmesoでは化学的に非等価、racemoでは等価になっています。
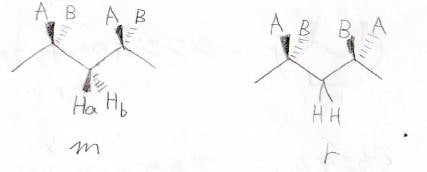
化学的な等価性についてはこちらの記事で解説しています。

この違いを¹H-NMRで読み取ることにより、mesoとracemoの割合、すなわち2連子タクティシティーを求めることができます。
結晶性
高分子の立体の違いは、結晶性に大きな違いを生じさせます。
そもそも結晶とは、分子が規則正しく並んだ相のことを言いますが、高分子では長い鎖が完全に並ぶことはとても難しいため、結晶部分と非晶部分(ガラス)が混ざったものにならざるを得ません。
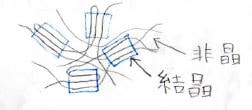
そのため、これを高分子結晶と呼びます。
さらに、側鎖が邪魔になってきれいに整列することができない場合、例えば、枝分かれ構造や架橋ネットワークなどでは結晶にならない、すなわち融点をもたない場合もあります。
その例として、ポリプロピレンではイソタクチック、シンジオタクチック、アタクチックで融点にこのような違いが生じます。

ここでi、s、aはそれぞれの立体規則性を指す頭文字です。
イソタクチックポリプロピレンの融点は約\(\displaystyle 160^\circ \rm{C}\)、シンジオタクチックポリプロピレンは約\(\displaystyle 140^\circ \rm{C}\)になります。
そして、アタクチックポリプロピレンには融点がありません。
高分子は気体にならないので、融点をもたない場合は常に液体かと思うかもしれませんが、ガラス状態はあります。
実際に電子レンジでの加熱が可能なタッパーには結晶化しないガラス状態のポリプロピレンが使われていることが多いです。
なぜ結晶になっていないことがわかるかというと、透明性が高いからです。
結晶であれば異方性があって、光の干渉、全反射が起こります。
透明であるということは等方的であるということなので、それが結晶ではないことがわかります。
余談(耐熱性ペットボトル)
ちなみに、熱いお茶などを入れる耐熱性ペットボトルは少し結晶化しています。
一般的に融点はガラス転移温度よりも高いので、熱い飲み物を入れてガラスが融液状態になったとしても、まだ結晶が残っているのでボトルの形を保つことができます。
冷たいものを入れるペットボトルに比べて白く濁っているので、ぜひ確認してみてください。
製造の工程で、飲み口が最も結晶化するので、飲み口は真っ白になります。
らせん構造
最後に紹介する立体規則性による物性は、らせん構造です。
当たり前ですが、きれいにらせんを巻くためには、ランダムな立体構造は適していません。
たんぱく質のα-ヘリックス構造
その例として挙げられるのはまず、たんぱく質の\(\displaystyle \alpha\)-ヘリックス構造です。
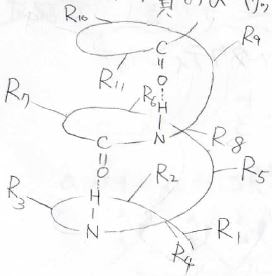
構成単位の\(\displaystyle \alpha\)-アミノ酸には不斉炭素があり、生体内のほとんどはL体です。
それらが酵素によって連鎖的に縮合していったものには完全な立体規則性があり、これによりきれいならせんを巻くようになります。
このらせん構造は、ペプチド結合の窒素原子上の水素とカルボニル酸素の間で水素結合ができることで安定なものになります。
側鎖はこのらせんの外側に配置されます。
溶液中のシンジオタクチックポリメタクリル酸メチル
そして、らせんの2つ目の例は溶液中のシンジオタクチックメタクリル酸メチル(sPMMA)です。

PMMAのように嵩高い側鎖をもつ高分子には、その立体反発を避けるためにらせんに近い構造をとろうとするものがあります。
とは言っても、\(\displaystyle \alpha\)-ヘリックスのように大きな安定化が起こるわけではないので、完全ならせん構造というよりは、くるんと巻いてるくらいのイメージです。
なお、らせん構造には右向きと左向きがあり、両者は鏡写しの関係なので、らせん状態では光学活性となります。
まとめ
今回の内容は以上です。
間違いの指摘、リクエスト、質問等あれば、Twitter(https://twitter.com/bakeneko_chem)かお問い合わせフォームよりコメントしてくださると、助かります。
それではどうもありがとうございました!